第三节 酸碱滴定
一、指示剂的作用原理
指示剂的作用原理是:指示剂的分子结构随pH的变化而发生结构互变,由于其共轭酸碱结构的颜色不同,从而引起溶液颜色的变化。
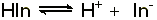
pH=pKHIn±1称为指示剂变色的pH范围
思考题:
某一酸碱指示剂的pKln=3.4,它的变色范围应是:
A.2.4~3.4
B.2.4~4.4
C.4.4~6.2
D.6.2~7.6
E.1.9~4.9
|
|
|
||
二、酸碱滴定曲线
思考题:
用 NaOH滴定液( 0.1000mol/L)滴定 20.00醋酸溶液时,应选用的指示剂为
A.甲基橙
B.酚酞
C.荧光黄
D.甲基红
E.铬黑 T
|
|
|
||
第四节 缓冲溶液
一、缓冲作用及缓冲溶液的概念
纯水或一般水溶液,常因外加酸碱或稀释而改变原有的pH值。但有一类溶液能抵抗外加的少量强酸、强碱和稍加稀释,而保持值基本不变。这种溶液称为缓冲溶液。缓冲溶液对强酸、强碱或稀释的抵抗作用称为缓冲作用。
缓冲溶液之所以具有缓冲作用,是由于在缓冲溶液中含有足量的抗酸和抗碱两种成分,通常把这两种成分称为缓冲对或缓冲系。
缓冲对为共轭酸碱对。由弱酸及共轭碱或弱碱及其共轭酸组成。
抗酸成分-共轭碱(弱酸盐)
抗碱成分-共轭酸(弱碱盐)
1.弱酸及其共轭碱
抗碱成分(弱酸) 抗酸成分(共轭碱)
HAc NaAc
H3PO4 NaH2PO4
H2CO3 NaHCO3
NaH2PO4 Na2HPO4
2.弱碱及其共轭酸
抗酸成分(弱碱) 抗碱成分(共轭酸)
NH3H2O NH4Cl
C6H5NH2 C6H5NH2HCL
(苯胺) (苯胺盐酸盐)
二、缓冲作用原理
以HAc-NaAc组成缓冲溶液为例,说明缓冲原理:
HAc+H2O
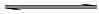
NaAc
上述反应中NaAc为强电解质,完全以Na+、Ac-存在于溶液中,HAc在溶液中由于同离子效应使之几乎完全以分子状态存在。所以在HAc~NaAc溶液中存有大量的HAc和Ac-,当加入少量酸时,溶液中Ac-接受质子平衡向生成HAc的方向(向左)移动,故溶液pH不明显改变。
三、缓冲容量和缓冲范围
缓冲溶液的缓冲容量取决于总浓度及缓冲比。
当缓冲比为定值时,总浓度愈大,则缓冲容量愈大。
当缓冲比等于1时,缓冲溶液的缓冲容量最大。
当缓冲比在1/10和10/1之间时,溶液pH=pKa
此时溶液具有较大的缓冲能力,称为缓冲溶液的缓冲范围。
缓冲溶液的缓冲范围:pH=pKa±1
思考题:
药物的pKa值是指其
A.90%解离时的pH值
B.99%解离时的pH值
C.50%解离时的pH值
D.10%解离时的pH值
E.全部解离时的pH值
|
|
|
||
四、缓冲溶液的配制
1.选择合适的缓冲对,使所选缓冲对中共轭酸的pKa与欲配制的缓冲溶液的pH值尽可能相等或接近,偏离的数值不应超过缓冲溶液的缓冲范围。
2.要有一定的总浓度保证在缓冲溶液中含有足量的抗酸成分和抗碱成分。
一般在0.05~0.5mol·dm-3之间为宜。
3.为了使缓冲溶液具有较大的缓冲容量,应尽量使缓冲比接近于1。
4.所选择的缓冲系不能与反应物或生成物发生作用。
思考题:
用酸度计测定溶液的pH值,测定前应用pH值与供试液较接近的一种标准缓冲液,调节仪器旋钮,使仪器pH示值与标准缓冲液的pH值一致,此操作步骤称为
A.调节零点
B.校正温度
C.调节斜率
D.平衡
E.定位
|
|
|
||
五、人体的缓冲体系和正常pH值的维持
人体血液中有一个缓冲能力很强的的缓冲系,并有肾肺的调节作用使血液pH维持 7.35~7.45之间 。
血浆中的缓冲系主要有:H2CO3~HCO3-、H2PO4-~HPO42-和血浆蛋白-血浆蛋白钠,在血浆中H2CO3主要以溶解的形式存在,有下述平衡: